5-Fu血藥濃度與藥代動(dòng)力學(xué)參數AUC分布除去個(gè)別患者退組者(因患者治療后期依從性不高��,部分患者未進(jìn)行后續治療��,對照組3例�,實(shí)驗組3例)���,37例對照組在6個(gè)周期內共計23次落在治療窗(AUC: 20~30mg·h /L)?的患者比例為16.67%(23/138) �����,多數患者的5-Fu AUC值都低于治療窗范圍����。實(shí)驗組基于 BSA 給藥后�����,患者的5-Fu血藥濃度分布也比較分散��,第1周期落在治療窗范圍內的患者比例為21.6%(8/37) �,其變異系數(CV) 48.77%�����,經(jīng)過(guò)2~6周期的劑量調整后�,到第6周期時(shí)比例提升到67.74%(23/34)���,其CV為22.75%���。兩組間差異有統計學(xué)意義(χ2=20.04����,P<0.01) ���。對照組和實(shí)驗組6個(gè)周期內5-Fu血藥濃度分析結果見(jiàn)圖 1�。
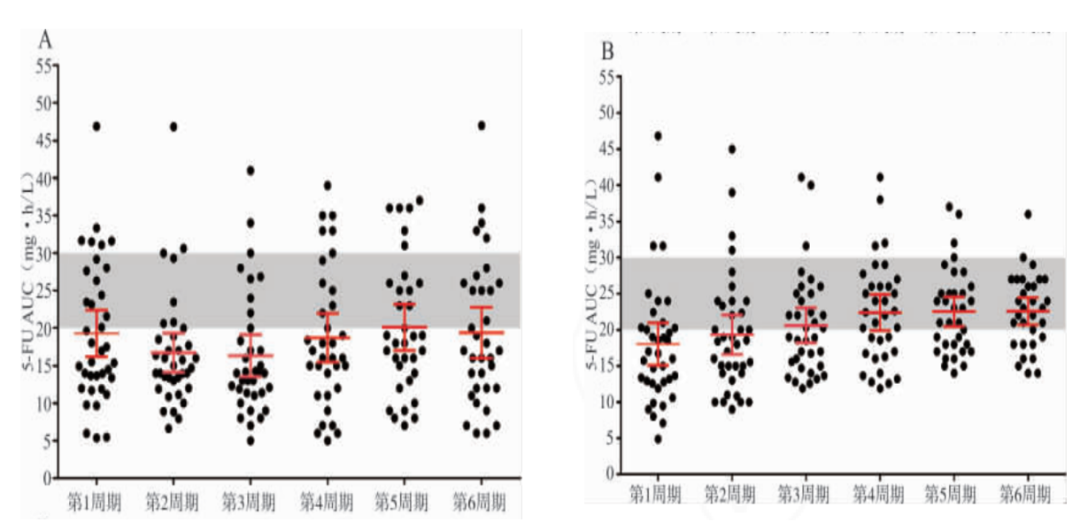
注:A����,對照組多數患者的5-Fu AUC 值低于治療窗范圍�。B�����,實(shí)驗組患者5-Fu血藥濃度落在治療窗范圍內的數量增加���,且具有集中趨勢[5]�����。圖 1 對照組和實(shí)驗組患者6個(gè)周期 5-Fu AUC 分布情況
5-Fu毒副反應與劑量調整的關(guān)系與對照組[70.3%( 26 /37) ]相比���,實(shí)驗組毒副反應(≥3級) 發(fā)生率[32.4% (12/37)]差異有統計學(xué)意義(χ2=10.60����,P<0.01) �����。進(jìn)一步分析具體的毒副反應結果表明��,腹瀉����、口腔黏膜炎等毒副反應的差異均有統計學(xué)意義(P均<0.05) ���,而惡心��、嘔吐����、手足綜合征��、食欲下降�、體重下降��、白細胞減少等差異均無(wú)統計學(xué)意義(P均>0.05)
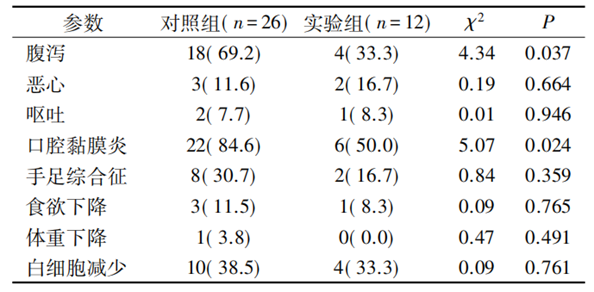
對照組與實(shí)驗組毒副反應的關(guān)系[n(%)]
大量針對西方人群的臨床試驗[6-7]表明�����,5-Fu的藥理特性與臨床毒性以及療效具有明顯的統計學(xué)相關(guān)性���,而體表面積給藥劑量與療效及總生存期差異均無(wú)統計學(xué)意義�����。這些臨床試驗表明���,在結直腸癌治療領(lǐng)域中�,通過(guò)對5-Fu常規血藥濃度監測�,并根據每例患者的藥理表征進(jìn)行個(gè)體化劑量調節�,能夠實(shí)現降低毒性����,增加治療效果的目的���。5-Fu的有效治療濃度范圍(治療窗) 非常窄�����,患者對藥物的代謝差異���,能引起個(gè)體藥效學(xué)上的巨大差異�。因此����,臨床迫切需要基于個(gè)體藥理差異對5-Fu進(jìn)行血藥濃度監測及劑量調節[8]�����。
通過(guò)本研究結果對比可知�,通過(guò)5-Fu血藥濃度檢測��,及時(shí)調整患者的用藥劑量��,可以使實(shí)驗組落在治療窗范圍內的患者比例明顯增加�����,表明通過(guò)藥代動(dòng)力學(xué)進(jìn)行5-Fu的劑量管理是一種臨床可行的操作�。改變用藥劑量可能會(huì )帶來(lái)化療毒副反應增加的風(fēng)險��,但是本研究結果表明����,通過(guò)劑量調整使得患者達到設定的治療窗血藥濃度范圍�����,不僅治療的效果沒(méi)有降低�,反而在整體的毒性控制更優(yōu)于BSA給藥方式����。此外��,本研究中以5-Fu為基礎的腸癌治療方案中�����,在引起白細胞減少癥方面差異無(wú)統計學(xué)意義(對照組為38.5%����,實(shí)驗組為33.3%) ����,這與國外文獻的報道的結論類(lèi)似[9]�����。
本研究亦證實(shí)通過(guò)監測患者化療過(guò)程中的5-Fu血藥濃度��,可以預估患者本次化療的毒副反應發(fā)生情況����,盡早予以干預���。由于檢測的是5-Fu在靜脈持續滴注過(guò)程中的血藥濃度�,因此��,可以根據及時(shí)的檢測報告來(lái)預判本次5-Fu后續持續滴注過(guò)程中的代謝情況��,進(jìn)而可以依據患者自身狀態(tài)及檢測結果適當的進(jìn)行滴注持續時(shí)間的調整�,以控制化療相關(guān)毒性反應或者提高化療的療效��。